Оперативный контроль параметров качества лежит в основе мониторинга системы качества и в рамках процессного подхода является эффективным инструментом реализации одного их принципов управления качеством – улучшения характеристик СМК.
Таким образом, исходя из определения, сформулированного Национальным стандартом Российской Федерации ГОСТ Р 52249-2004 «Правила производства и контроля качества лекарственных средств», а также документами международными организаций (например, PIC/S в Европе или FDA в США), контроль качества – это составная часть GMP, связанная с отбором проб, проведением испытаний и проверок на соответствие продукции требованиям спецификаций, а также с организацией, документированием и процедурами выдачи разрешений, гарантирующих, что необходимые и относящиеся к делу испытания действительно проведены, и что исходное сырье и материалы не разрешены для использования, а продукция не разрешена для продажи или поставки до тех пор, пока их качество не будет установленным образом признано удовлетворительным.
2.3.1. Условия осуществления контроля качества
Для осуществления на предприятии по производству лекарственных средств контроля качества в рамках системы обеспечения качества необходимо наличие соответствующей организационной структуры, штата, процессов, процедур, материально-технического и методического обеспечения, а также ресурсов.
2.3.1.1. Организационная структура
Первым и основным шагом при формировании структуры претворения в жизнь концепции контроля качества как составного элемента системы обеспечения качества является создание отдела контроля качества. При этом необходимо соблюдать фундаментальный принцип современного менеджмента – независимость контроля качества от производства. С учетом этого принципа место ОКК в органиграмме (структуре) предприятия можно представить в виде следующей схемы:
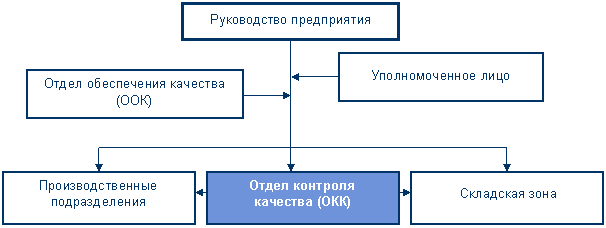
Из приведенной схемы следует, что в сфере оперативного (точечного) контроля на этапах входного и операционного контроля, контроля производства и персонала, а также контроля качества готовой продукции, ОКК является ближайшим и основным уровнем подчинения для отдела обеспечения качества (ООК), которому ОКК обязан представлять все необходимые сведения, в т.ч. документальные, по первому требованию, а по ряду согласованных и закрепленных в соответствующих нормативных документах позиций, в инициативном порядке.
В соответствии с представленной схемой начальник ОКК руководствуется в своей деятельности приказами, распоряжениями и поручениями руководства предприятия (директора), распоряжениями Уполномоченного лица и указаниями начальника ООК, которые подлежат неукоснительному исполнению. Основная цель, преследуемая подобной структуры подчинения в СМК – формирование у Уполномоченного лица уверенности в том, что «каждая серия продукции произведена и проверена в соответствии с установленными требованиями» (ГОСТ Р 52249-2004, п.1.2, VII, п.2.4, а). Лишь при наличии такой уверенности Уполномоченное лицо дает письменное разрешение на выпуск серии лекарственного средства в обращение, а его подпись на разрешении является гарантией соответствия качества данной серии регистрационному досье.